0 引言
1 材料与方法
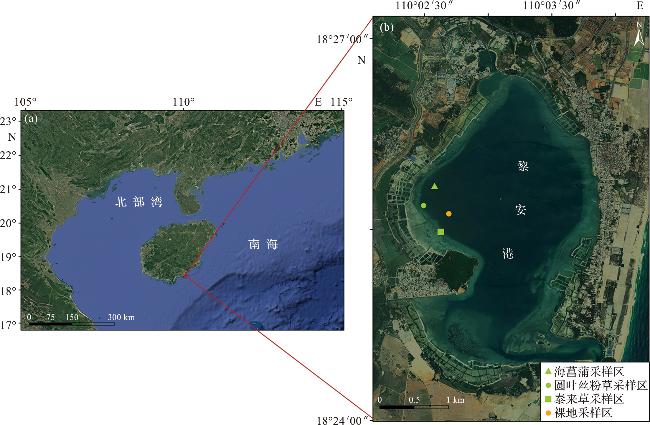
1.1 研究区域及样品采集
表1 黎安港沉积物柱样信息Tab.1 Information of sediment cores in Li’an Lagoon |
| 采集区域 | 柱样名称 | 柱样长度/cm | 分样数量/个 |
|---|---|---|---|
| 海菖蒲 分布区域 | LA-01 | 30 | 6 |
| LA-02 | 40 | 8 | |
| LA-03 | 40 | 8 | |
| 圆叶丝粉草 分布区域 | LA-04 | 45 | 9 |
| LA-05 | 50 | 10 | |
| LA-06 | 55 | 11 | |
| 泰来草 分布区域 | LA-07 | 60 | 12 |
| LA-08 | 60 | 12 | |
| LA-09 | 50 | 10 | |
| 裸地区域 | LA-10 | 55 | 11 |
| LA-11 | 50 | 10 | |
| LA-12 | 50 | 10 |
1.2 样品测定
1.3 数据分析
2 结果
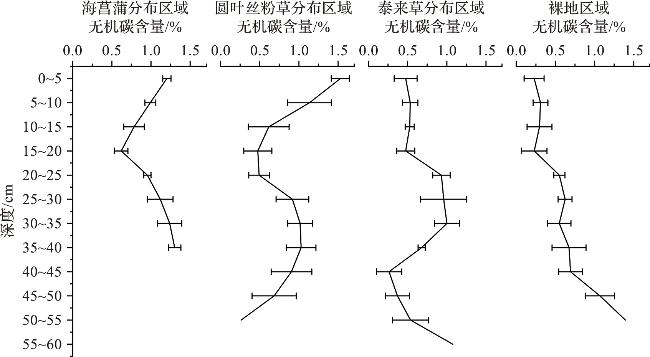
2.1 沉积物无机碳含量与单位面积储量的差异
表2 不同海草物种分布区域及裸地沉积物的无机碳密度与储量Tab.2 Inorganic carbon density and storage in sediments of different seagrass species distribution areas and bare areas |
| 采集区域 | 柱样名称 | 柱样无机碳密度a /(g·cm-3) | 区域无机碳密度b /(g·cm-3) | 表层沉积物单位面积无机 碳储量估算/(Mg·ha-1) |
|---|---|---|---|---|
| 海菖蒲分布区域 | LA-01 | 0.009 2±0.001 3 | 0.010 6±0.000 9 | 105.66±9.45 |
| LA-02 | 0.012 2±0.000 9 | |||
| LA-03 | 0.011 3±0.001 0 | |||
| 圆叶丝粉草分布区域 | LA-04 | 0.011 2±0.001 1 | 0.009 6±0.003 1 | 96.09±31.36 |
| LA-05 | 0.012 4±0.001 2 | |||
| LA-06 | 0.005 2±0.001 5 | |||
| 泰来草分布区域 | LA-07 | 0.007 0±0.001 0 | 0.007 5±0.000 8 | 75.05±8.17 |
| LA-08 | 0.0087±0.001 3 | |||
| LA-09 | 0.006 9±0.001 4 | |||
| 裸地区域 | LA-10 | 0.009 4±0.001 2 | 0.006 0±0.002 5 | 59.84±24.55 |
| LA-11 | 0.004 0±0.000 8 | |||
| LA-12 | 0.004 5±0.001 1 |
注:a.沉积物不同深度层间无机碳密度的显著性检验结果如下:海菖蒲分布区域差异显著(p=0.034;N=22),而圆叶丝粉草分布区域(p=0.173;N=30)、泰来草分布区域(p=0.079;N=33)及裸地区域(p=0.075;N=30)差异均未达到显著水平。b.不同区域之间(以柱样整体平均值为统计单元)沉积物无机碳密度差异均显著(p<0.05;N=12)。 |
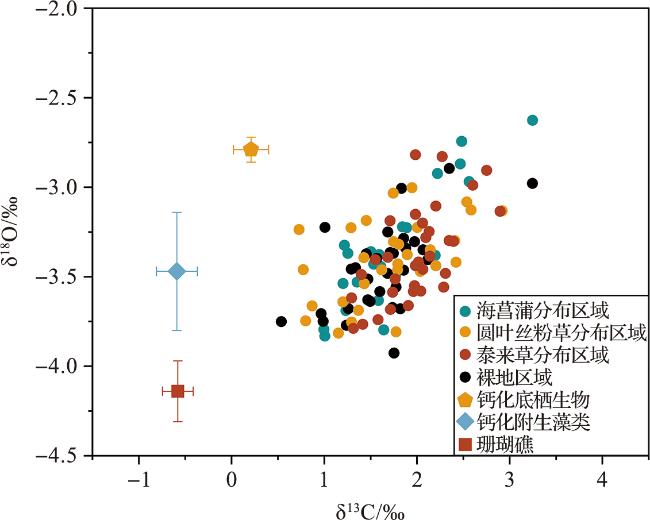
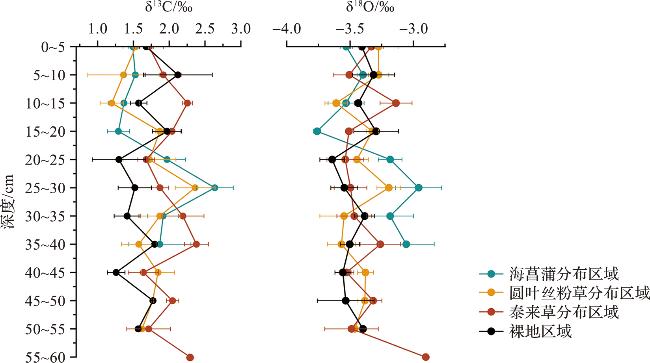
2.2 沉积物碳酸盐碳、氧同位素组成特征
3 讨论
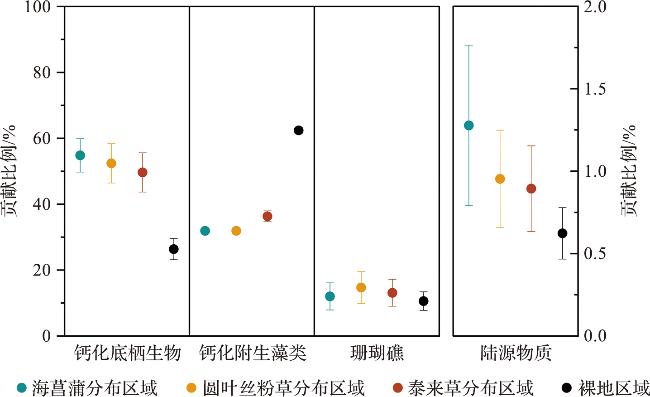
3.1 海草物种对海草床沉积物无机碳积累的影响
3.2 沉积物无机碳积累的关键环境驱动因素:碳、氧同位素证据
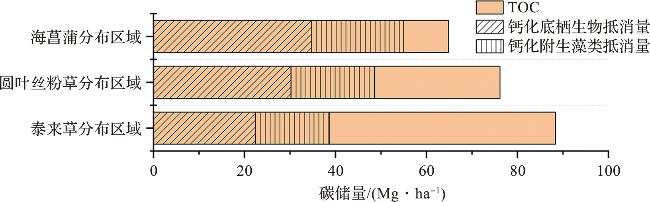
3.3 沉积物无机碳对海草床碳汇能力的影响
表3 不同区域与全球海草床有机碳/无机碳储量估算Tab.3 Estimation of organic/inorganic carbon stocks of seagrass meadows across different regions and globally |
| 区域 | 有机碳储量/ (Mg·ha-1) | 无机碳储量/ (Mg·ha-1) | 数据来源 |
|---|---|---|---|
| 巴西东南部 | 67.6±14.7 | 141.5±60.0 | 文献[5] |
| 佛罗里达湾(美国) | 175.0±20.4 | 754.6±26.7 | 文献[5] |
| 埃克苏马群岛 | 956±70.0 | 文献[29] | |
| 全球 | 120.8±3.5 | 654±24 | 文献 [9,25] |
| 海南黎安(海菖蒲) | 64.84±3.02 | 105.66±9.45 | 本研究 |
| 海南黎安(圆叶丝粉草) | 76.17±13.25 | 96.09±31.36 | 本研究 |
| 海南黎安(泰来草) | 88.37±4.91 | 75.05±8.17 | 本研究 |
注:所有数据均表征表层1 m沉积物储量。 |