0 引言
1 材料与方法
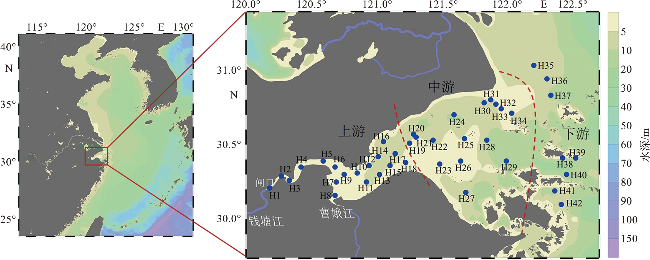
1.1 研究区域与站位分布
1.2 水体溶解N2O采集与测定
1.3 其他参数采集与测定
1.4 N2O浓度和饱和度计算
1.5 耗氧量计算
1.6 海-气交换通量评估
2 结果与讨论
2.1 春季杭州湾及其邻近海域水体温、盐和水化学参数分布
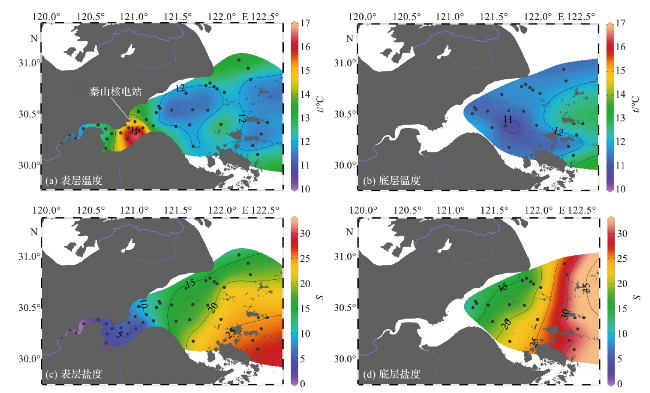
图2 春季杭州湾及其邻近海域水体温度和盐度的水平分布图Fig.2 Horizontal distribution of temperature and salinity in Hangzhou Bay and its adjacent waters in spring |
表1 春季杭州湾及其邻近海域水体温度、盐度和水文化学参数的平均值Tab.1 Average water temperature, salinity and hydrochemical parameters of Hangzhou Bay and its adjacent waters in spring |
| 项目 | 温度/℃ | 盐度 | c(NO3-)/ (μmol·L-1) | c(NH4+)/ (μmol·L-1) | c(NO2-)/ (μmol·L-1) | c(DIN)/ (μmol·L-1) | c(DO)/ (μmol·L-1) | c(N2O) / (nmol·L-1) | R(N2O)/% |
|---|---|---|---|---|---|---|---|---|---|
| 上游表层 | 13.6±1.6 | 4.6±3.4 | 146.5±13.8 | 4.1±3.5 | 2.6±1.3 | 153.2±14.6 | 17.2±2.9 | 151±17 | |
| 中游表层 | 12.0±0.4 | 16.7±3.2 | 83.6±19.0 | 0.8±0.3 | 0.3±0.3 | 84.8±19.0 | 305±8 | 14.1±0.8 | 125±6 |
| 中游底层 | 11.5±0.3 | 17.1±3.3 | 81.4±18.1 | 1.1±0.4 | 0.3±0.2 | 82.8±18.2 | 307±7 | 14.2±0.6 | 125±5 |
| 下游表层 | 12.1±0.7 | 22.2±5.2 | 50.9±17.5 | 1.2±1.0 | 0.4±0.4 | 52.5±18.7 | 295±14 | 13.2±0.7 | 123±6 |
| 下游底层 | 12.1±0.6 | 30.5±2.1 | 25.7±13.4 | 0.6±0.3 | 0.3±0.1 | 26.6±13.1 | 283±8 | 12.4±0.6 | 120±7 |
注:上游水体无实测DO数据。 |
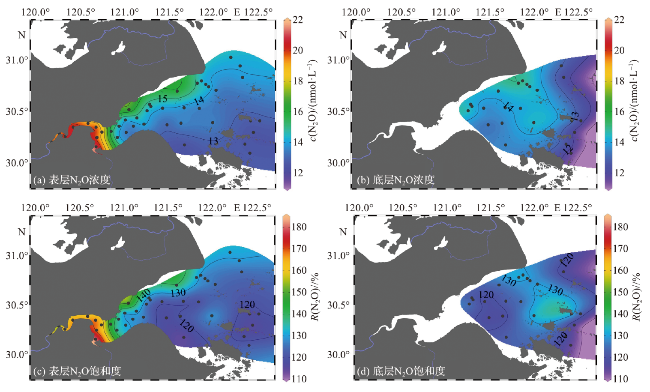
2.2 春季杭州湾及其邻近海域水体溶解N2O浓度和饱和度分布
2.3 春季杭州湾及其邻近海域水体N2O分布的影响因素
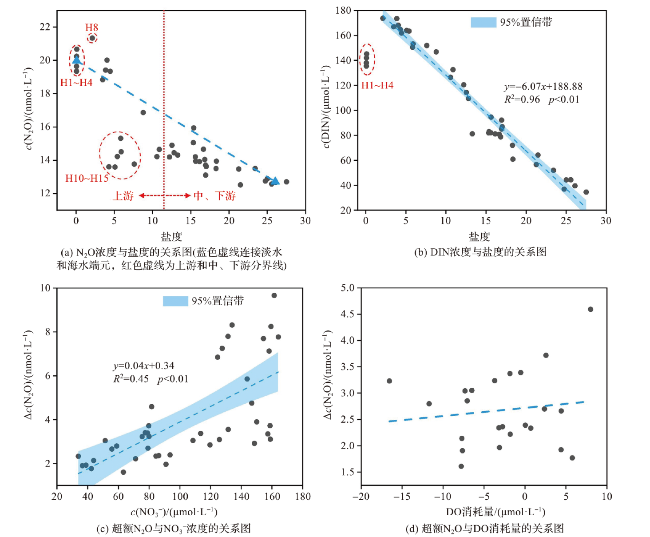
2.3.1 河流输入与河口混合
2.3.2 氮素营养盐输入和生物作用
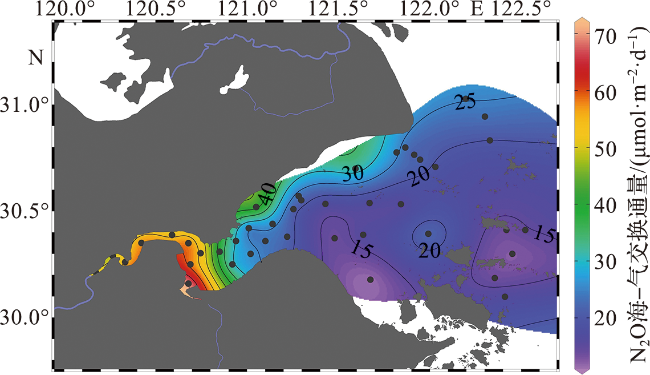
2.4 春季杭州湾及其邻近海域水体溶解N2O的海-气交换通量
表2 春季杭州湾及其邻近海域N2O的海-气交换通量与释放量Tab.2 Sea-air exchange flux and release of N2O in Hangzhou Bay and its adjacent waters in spring |
| 项目 | FBorges/(μmol·m-2·d-1) | FN2000/(μmol·m-2·d-1) | FW2014/(μmol·m-2·d-1) | 面积/km2 | N2O释放量/(mol·d-1) |
|---|---|---|---|---|---|
| 上游 | 43.0±15.6 | 39.5±14.3 | 34.7±12.5 | 1 250 | 0.5×105 |
| 中游 | 20.2±5.2 | 18.6±4.8 | 16.3±4.2 | 8 200 | 1.7×105 |
| 下游 | 17.5±4.9 | 16.1±4.5 | 14.1±3.9 | 7 600 | 1.3×105 |
注:FBorges,FN2000和FW2014分别表示用Borges公式、N2000公式和W2014公式计算的N2O海-气交换通量。 |
表3 国内不同河口、海湾表层水体溶解N2O的浓度、饱和度和海-气交换通量Tab.3 Concentrations, saturations and sea-air exchange fluxes of dissolved N2O in surface waters of different domestic estuaries and bays |
| 海域 | 调查时间 | N2O浓度/(nmol·L-1) | N2O饱和度/% | N2O海-气交换通量/(μmol·m-2·d-1) | 文献 |
|---|---|---|---|---|---|
| 渤海湾 | 2020年7月 | 32.5±7.0 | 495.1±101 | 25.9±6.7a;32±8.27b | [45] |
| 2020年10月 | 23.2±6.5 | 249.8±80.4 | 22.1±13.3a;19.1±11.5b | [45] | |
| 胶州湾 | 2006年8月 | 8.10±1.38 | 122±20 | 1.37±1.24c;3.31±3.00d | [46] |
| 2006年12月 | 32.26±13.15 | 294±120 | 27.18±16.85c;53.28±33.03d | [46] | |
| 2007年4月 | 17.37±2.65 | 172±29 | 6.83±2.69c;14.38±5.66d | [46] | |
| 2007年10月 | 12.11±0.48 | 143±7 | 3.41±0.55c;7.59±1.23d | [46] | |
| 桑沟湾 | 2013年4月 | 11.77±0.52 | 99.21±2.85 | -0.41±1.37c-0.48±2.86d | [47] |
| 2013年7月 | 10.47±0.61 | 137.99±6.26 | 2.26±0.37c;4.48±0.73d | [47] | |
| 2013年10月 | 10.59±1.02 | 129.76±12.83 | 0.16±0.13c;0.81±0.86d | [47] | |
| 2014年1月 | 17.98±1.94 | 128.01±11.97 | 0.11±0.12c;0.54±0.94d | [47] | |
| 新村湾 | 2020年7月 | 5.52±0.50 | 100±9 | 0.01±0.09c;0.10±0.53d | [48] |
| 2021年1月 | 7.11±0.84 | 88±11 | -0.07±0.12c;-0.31±0.70d | [48] | |
| 长江口 | 2011年3月 | 11.1 | 107 | 0.01a;0.001b | [24] |
| 2011年5月 | 10.1±0.7 | 122±7 | 4.4±5.9a;4.4±6.3b | [24] | |
| 2011年8月 | 10.2±0.7 | 153±10 | 9.1±5.3a;8.7±5.5b | [24] | |
| 2011年10月 | 7.7±0.6 | 99±5 | 0.2±1.2a;0.2±1.2b | [24] | |
| 2012年3月 | 13.27±6.40 | 111.5±41.4 | 3.2±10.9c;5.5±19.3d;12.2±52.3f | [49] | |
| 2012年7月 | 10.62±5.03 | 155.9±68.4 | 7.3±12.4c;12.7±20.4d;20.4±35.9f | [49] | |
| 珠江口 | 2010年3月 | 8.0~329.0 | 112~3 799 | 2.0~637.0e | [50] |
| 2010年8月 | 8.0~97.0 | 138~1 477 | 0.1~227.0e | [50] | |
| 2011年1月 | 9.0~283.0 | 115~2 740 | 2.0~519.0e | [50] | |
| 九龙江口 | 2020年7月 | 15.3~44.9 | 462.7±167.2 | 13.0~57.0f | [51] |
| 2020年12月 | 17.9~50.2 | 400.5±132.9 | 13.6~61.0f | [51] | |
| 杭州湾 | 2022年3月 | 15.2±2.7 | 136±18 | 29.5±16.0e;27.1±14.7a;23.8±12.9b | 本研究 |