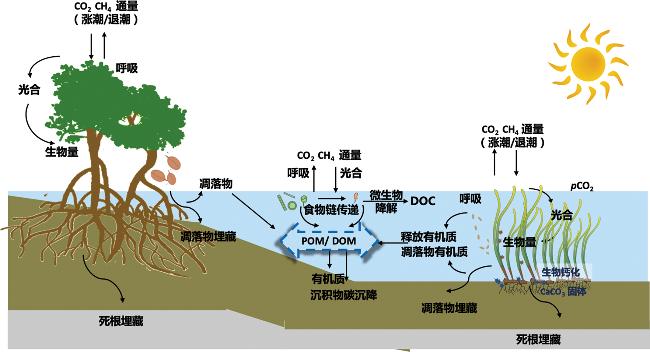
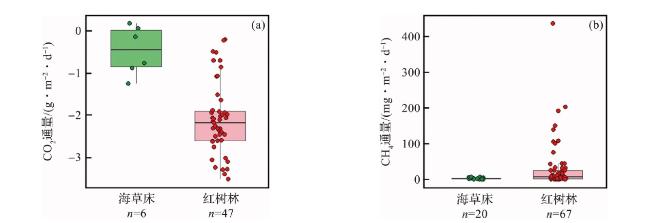
红树林虽被誉为滨海湿地最大的碳库
[72],但其固定的碳有相当一部分通过潮汐运动、孔隙水排放以及凋落物掉落等过程输出到邻近的水体中
[73]。在潮汐作用下,红树林以POC等形式向近岸海水输出的碳量,可占其沉积物固碳总量的50%以上
[72,74]。例如,在澳大利亚Missionary Bay,涡度相关-潮位同步观测系统的数据显示,红树林向海草床输出的POC瞬时通量可达44±9 g·m
-2·d
-1,相当于同期红树林净生态系统生产(net ecosystem production,NEP)的53%
[10]。在亚马孙河口,红树林输出的DOC浓度高达6.3±1.7 mmol·L
-1,其浓度沿盐度梯度呈指数衰减,半衰减距离约为8.5 km,这些DOC直接支撑了下游海草床的异养呼吸过程
[75]。此外,红树林根系呼吸和硫酸盐还原过程释放的DIC(平均浓度为3.9 mmol·L
-1)可通过密度流沿潮沟底部向海草床输送,形成“暗碳”通道
[46]。若忽视这些横向碳输出,可能导致区域尺度上红树林碳汇估算偏高30%~110%
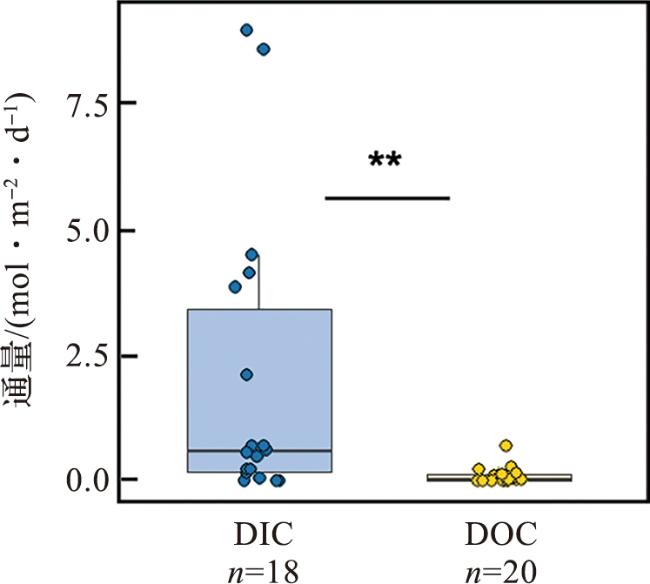
[76]。大量研究表明,DIC是红树林与邻近生态系统碳交换的主要形态
[77-79],红树林通过地下水交换输出的DIC和DOC通量分别为1.99±0.67 mol·m
-2·d
-1(
n=18)和0.12±0.04 mol·m
-2·d
-1(
n=20)(
图3)。全球红树林DIC输出通量为(1.03~2.23)×10
13mol·a
-1,约占全球河流向海洋输送DIC总量的46%
[80]。全球红树林DIC和DOC通量远大于红树林碳埋藏总量(3.42×10
12 mol·a
-1)
[81]。因此,横向输出的DIC是红树林生态系统不可忽视的碳输出(
图4)。最新一项涵盖东南亚12个河口区的研究指出,将横向输出(POC+DOC+DIC)纳入碳收支后,红树林净生态系统碳平衡(net ecosystem carbon balance,NECB)平均下调46%
[17]。由于红树林与其他蓝碳生态系统间的碳交换通常基于碳储量与总生产力之间的差值间接估算,而现有研究缺乏对连续体间碳交换过程的解析,这可能导致红树林碳汇潜力的高估超过一半
[76]。