0 引言
1 海岸海洋碳循环过程
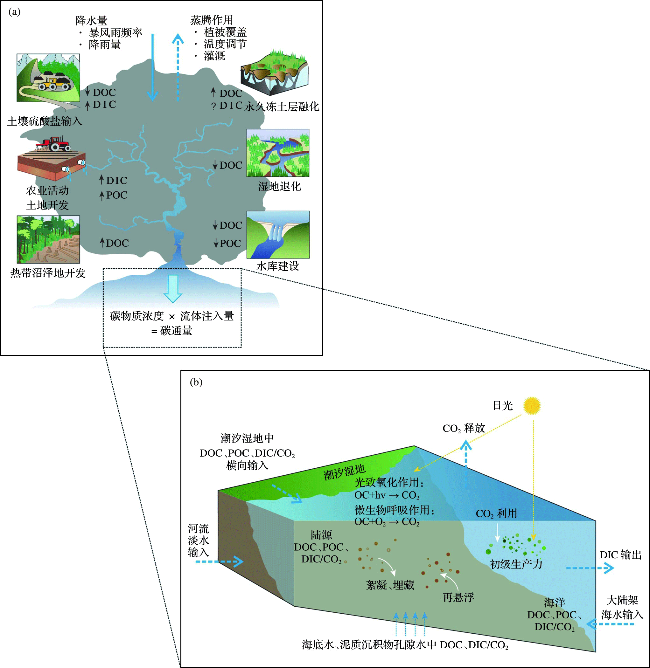
图1 海岸海洋中有机碳和无机碳通量的影响因素及碳循环过程(图片修改自文献[10]。其中DOC、DIC、POC和hv分别代表溶解有机碳、溶解无机碳、颗粒有机碳和光子能量。) Fig.1 Influencing factors of organic carbon and inorganic carbon fluxes and carbon cycle processes in coastal ocean (Figure was modified from reference[10]. DOC, DIC, POC and hv are dissolved organic carbon, dissolved inorganic carbon, particulate organic carbon and photon energy, respectively.) |
1.1 潮汐湿地
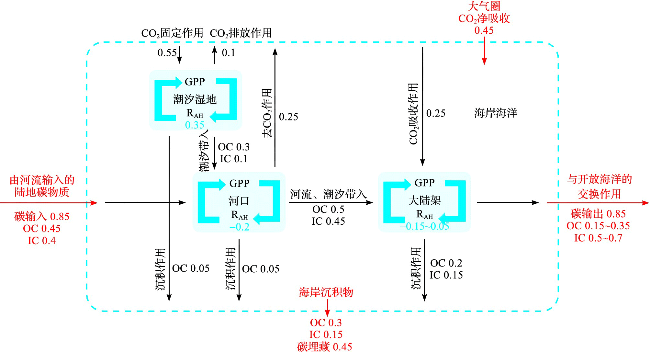
图2 海岸海洋系统中潮汐湿地、河口和大陆架3个子系统中的有机碳和无机碳通量统计及其输送方向(图片修改自文献[10]。OC为有机碳,IC为无机碳,红色数值代表海岸海洋系统与外部系统交换的碳通量,黑色数值代表海岸海洋系统内部交换的碳通量,箭头指示碳的输送方向,所有OC和IC通量均为正值。蓝色数值代表初级生产总量(GPP)和系统呼吸作用总量(RAH)之间的平衡量,即净生态系统生产力(NEP),负值表示OC转化为IC的碳通量。碳通量误差忽略不计。图中数值单位为Pg C·a-1。) Fig.2 Statistic data of organic carbon and inorganic carbon fluxes in the three subsystems of tidal wetlands, estuarine and continental shelf in coastal marine system and their transport directions (Figure was modified from reference[10]. OC is organic carbon, IC is inorganic carbon. Red and black values are the carbon fluxes exchanged across and within the boundaries of the coastal ocean, with positive values. Arrows indicate the directions of the carbon matters transport. Blue values represent the balance between gross primary production (GPP) and total system respiration (RAH), i.e., net ecosystem production (NEP), with negative values indicating conversion of OC to IC. Carbon flux error is negligible. The unit is Pg C·a-1.) |
1.2 河口
1.3 大陆架
1.4 海-气相互作用
2 海岸海洋CO2通量的影响因素及变化机理
2.1 海岸海洋CO2通量的影响因素
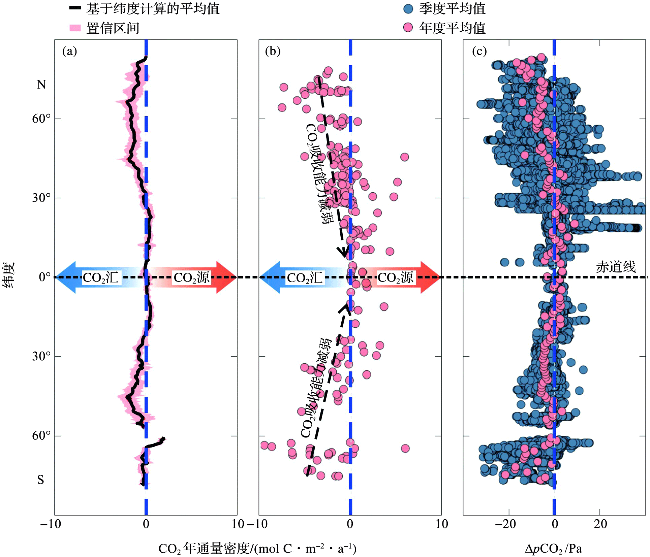
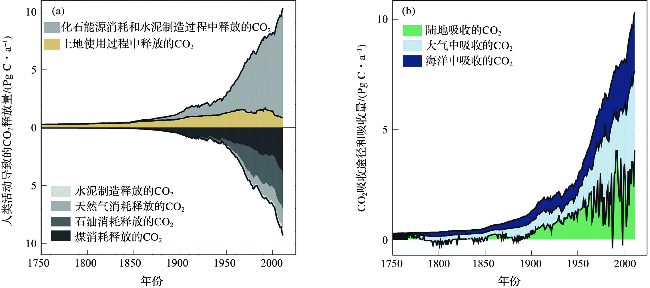
图3 CO2年通量密度与海岸海洋所处纬度的关系(a);据文献数据汇编的CO2年通量密度与海岸海洋所处纬度的关系(b);距离世界范围内主要陆地50 km处的季节性和年平均ΔpCO2(c)Fig.3 The relationship between annual CO2 flux density and the coastal ocean latitude(a); The relationship between annual CO2 flux density and coastal ocean latitude, compiled from the literatures(b); Seasonal and annual mean ΔpCO2 at 50 km from land(c) (Figure was modified from reference[43].The data of fig.a were from reference[20].) |
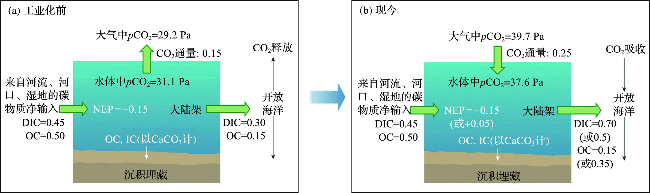
图4 工业化前和现今大陆架的有机碳和无机碳通量、 pCO2水平以及生态系统净产量(图片修改自文献[10]。图中有机碳和无机碳通量以及生态系统净产量的单位为Pg C·a-1。) Fig.4 pCO2 levels, net ecosystem production (NEP), and organic and inorganic carbon fluxes on pre-industrial and current continental shelves (Figure was modified from reference[10]. The unit for organic carbon, inorganic carbon fluxes and NEP in this figure is Pg C·a-1.) |
2.2 CO2通量变化机理
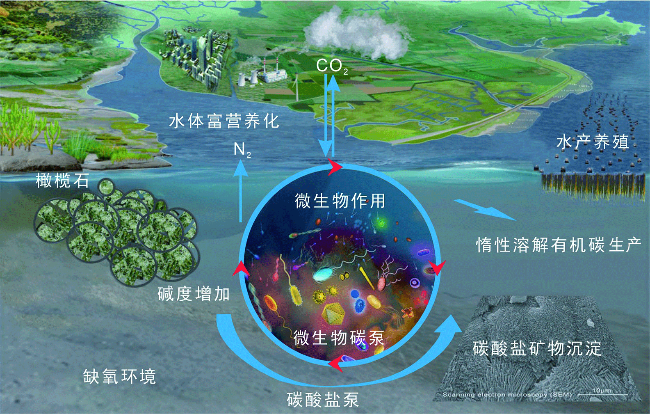
图6 缺氧环境中以微生物和流体-岩石相互作用为媒介的海洋负碳排放(ONCE)过程(图片修改自文献[21]。ONCE包括惰性溶解有机碳生产、碱度增强和碳酸盐矿物沉淀。) Fig.6 Ocean carbon negative emission (ONCE) processes mediated by microbial and fluid-rock interactions in anoxic environments (Figure was modified from reference[21]. ONCE including refractory dissolved organic carbon production, alkalinity enhancement, and carbonate minerals precipitation.) |