0 引言
1 材料与方法
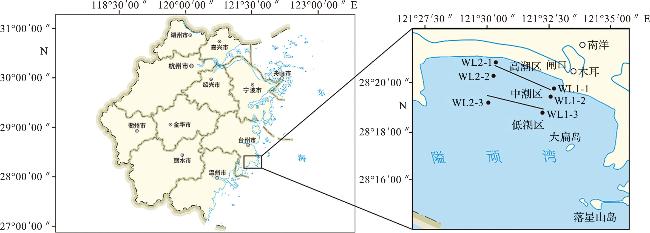
1.1 调查区域与站位布设
1.2 样品采集及处理
1.3 微藻群落结构分析
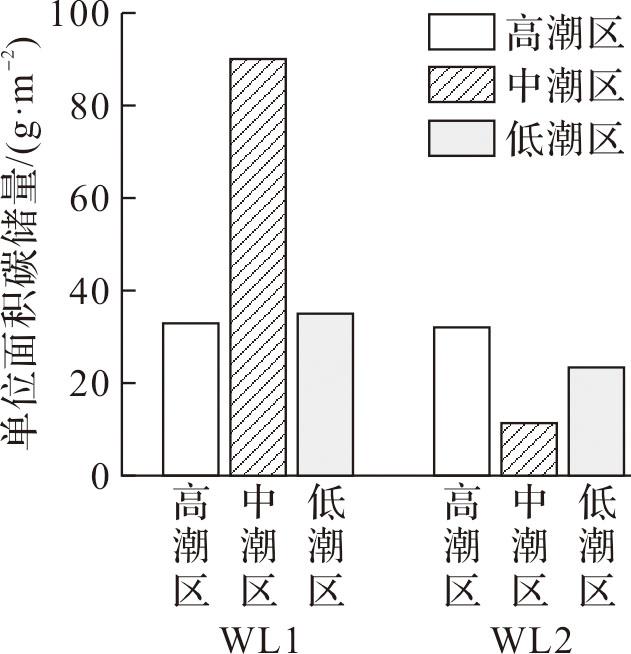
1.4 生物量及碳库计算
2 结果与讨论
2.1 微藻的群落构成与生态类型
表1 隘顽湾泥滩微藻主要优势种丰度与生物量Tab.1 Abundance and biomass of the main species of microalgae in the mudflat of Aiwan Bay |
| 优势种 | 丰度/(×103 cells·cm-3) | 丰度占比/% | 生物量/(μg·cm-3) | 生物量占比/% | |
|---|---|---|---|---|---|
| 辐射列圆筛藻 Coscinodiscus radiatus | 0.84±0.54 | 10.43 | 1.00±0.64 | 13.32 | |
| 钝头菱形藻 Nitzschia obtusa | 钝头菱形藻 Nitzschia obtusa | 0.50±0.66 | 6.16 | 0.28±0.37 | 3.76 |
| 弯菱形藻 Nitzschia sigma | 0.42±0.34 | 5.21 | 0.06±0.05 | 0.84 | |
| 小眼圆筛藻 Coscinodiscus oculatus | 0.35±0.17 | 4.30 | 0.37±0.19 | 4.98 | |
| 长尾布纹藻 Gyrosigma macrum | 0.33±0.26 | 4.06 | 0.05±0.04 | 0.73 | |
| 长端节肋缝藻 Frustulia lewisiana | 0.32±0.37 | 4.01 | 0.26±0.29 | 3.45 | |
| 波状辐裥藻 Actinoptychus undulates | 0.27±0.19 | 3.38 | 0.12±0.08 | 1.64 | |
| 波罗的海布纹藻 Gyrosigma balticum | 0.28±0.17 | 3.48 | 0.45±0.27 | 6.06 | |
| 斜纹藻 Pleurosigma spp. | 0.24±0.18 | 2.97 | 0.26±0.20 | 3.56 | |
| 平片针杆藻 Synedra tabulata | 0.24±0.33 | 2.93 | 0.03±0.04 | 0.39 | |
| 星脐圆筛藻仿玟纹变种 Coscinodiscus asteromphalus var. subbuliens | 0.21±0.11 | 2.54 | 0.56±0.30 | 7.47 | |
| 小等刺硅鞭藻 Dictyocha fibula | 0.22±0.19 | 2.70 | 0.46±0.40 | 6.07 | |
| 流水双菱藻 Surirella fluminensis | 0.20±0.12 | 2.47 | 0.15±0.10 | 2.07 | |
| 中肋骨条藻 Skeletonema costatum | 0.58±1.18 | 7.23 | 0.02±0.05 | 0.31 | |
| 斯氏布纹藻 Gyrosigma spencerii | 0.20±0.19 | 2.54 | 0.03±0.03 | 0.46 |
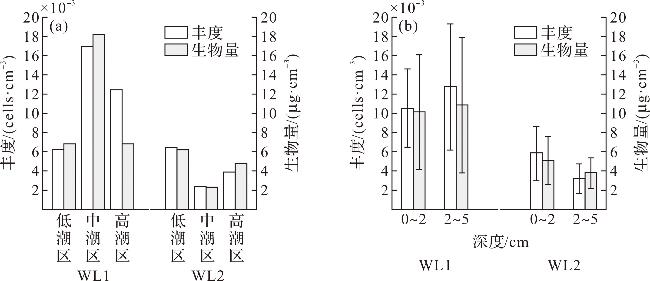
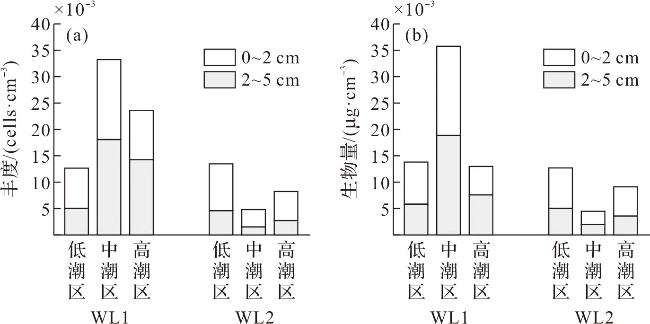
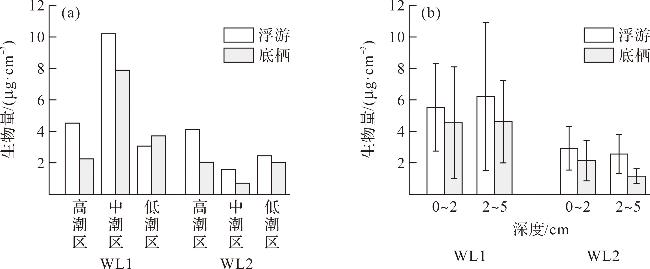
2.2 微藻各类群的数量组成与分布
表2 隘顽湾泥滩微藻各类群的平均丰度与生物量Tab.2 Average abundances and biomass among microalgal taxonomic groups in the mudflat of Aiwan Bay |
| 种类 | 平均丰度/(×103cells·cm-3) | 丰度占比/% | 平均生物量/(μg·cm-3) | 生物量占比/% |
|---|---|---|---|---|
| 硅藻 | 7.67±5.34 | 95.44 | 6.68±4.84 | 89.94 |
| 金藻 | 0.23±0.21 | 2.85 | 0.47±0.43 | 6.34 |
| 甲藻 | 0.05±0.05 | 0.65 | 0.27±0.28 | 3.60 |
| 绿藻 | 0.09±0.10 | 1.06 | 0.01±0.01 | 0.12 |
| 合计 | 8.04±5.55 | 100 | 7.42±5.51 | 100 |
2.3 多样性指数和均匀度指数
表3 隘顽湾泥滩不同潮区微藻的多样性指数和均匀度指数Tab.3 Diversity and evenness indices of microalgae in different tidal zones in the mudflat of Aiwan Bay |
| 指数 | WL1断面 | WL2断面 | |||||
|---|---|---|---|---|---|---|---|
| 高潮区 | 中潮区 | 低潮区 | 高潮区 | 中潮区 | 低潮区 | ||
| H'a | 3.24 | 3.46 | 3.23 | 3.32 | 2.95 | 3.14 | |
| H'b | 3.32 | 3.20 | 2.94 | 3.00 | 2.59 | 2.84 | |
| J'a | 0.84 | 0.89 | 0.86 | 0.87 | 0.84 | 0.83 | |
| J'b | 0.86 | 0.82 | 0.78 | 0.79 | 0.74 | 0.76 | |
表4 隘顽湾泥滩不同深度微藻的多样性指数和均匀度指数Tab.4 Diversity and evenness indices of microalgae at different depths in the mudflat of Aiwan Bay |
| 指数 | WL1断面 | WL2断面 | |||
|---|---|---|---|---|---|
| 0~2 cm | 2~5 cm | 0~2 cm | 2~5 cm | ||
| H'a | 3.47 | 3.51 | 3.41 | 3.10 | |
| H'b | 3.18 | 3.29 | 3.07 | 2.74 | |
| J'a | 0.87 | 0.87 | 0.89 | 0.82 | |
| J'b | 0.80 | 0.81 | 0.80 | 0.72 | |